Die Einhaltung regulatorischer Vorschriften wird immer komplexer. Wir unterstützen Sie dabei, frühzeitig zu beginnen und sich gründlich auf die Dokumenteneinreichung vorzubereiten. Profitieren Sie von unserer (CTIS) Erfahrung und der gut etablierten Kommunikation mit den Prüfstellen.
Regulatory Affairs
Genehmigung Ihrer Studie in kürzester Zeit
EU/EEA: Verwaltung einer klinischen Studie über CTIS
Die Einreichung über CTIS ist bei uns seit dem 31. Januar 2023 obligatorisch.
Vereinfachung des regulatorischen Prozesses
Unsere Erfahrung
Einreichungen von klinischen Prüfungsanträgen über CTIS, Anfragen (RFIs) werden bei uns natürlich innerhalb der Frist beantwortet
CTIS-Einreichungen werden gründlich durchgeführt
Unsere Experten für regulatorische Angelegenheiten werden stetig intensiv geschult und auch unser gesamtes Team erhalten grundlegende Trainings
Besser eine Woche für die Planung hinzufügen, als einen Monat für Überarbeitungen verschwenden
Um die Prüf- und Genehmigungsfristen zu verkürzen und unnötige Anfragen zu vermeiden, ist die Einreichung eines vollständigen und qualitativ hochwertigen Dossiers von besonderer Bedeutung
Vermeiden Sie last-minute Änderungen und Entscheidungen
Wir setzten proaktive Anfragen um, bevor die Zentren danach fragen
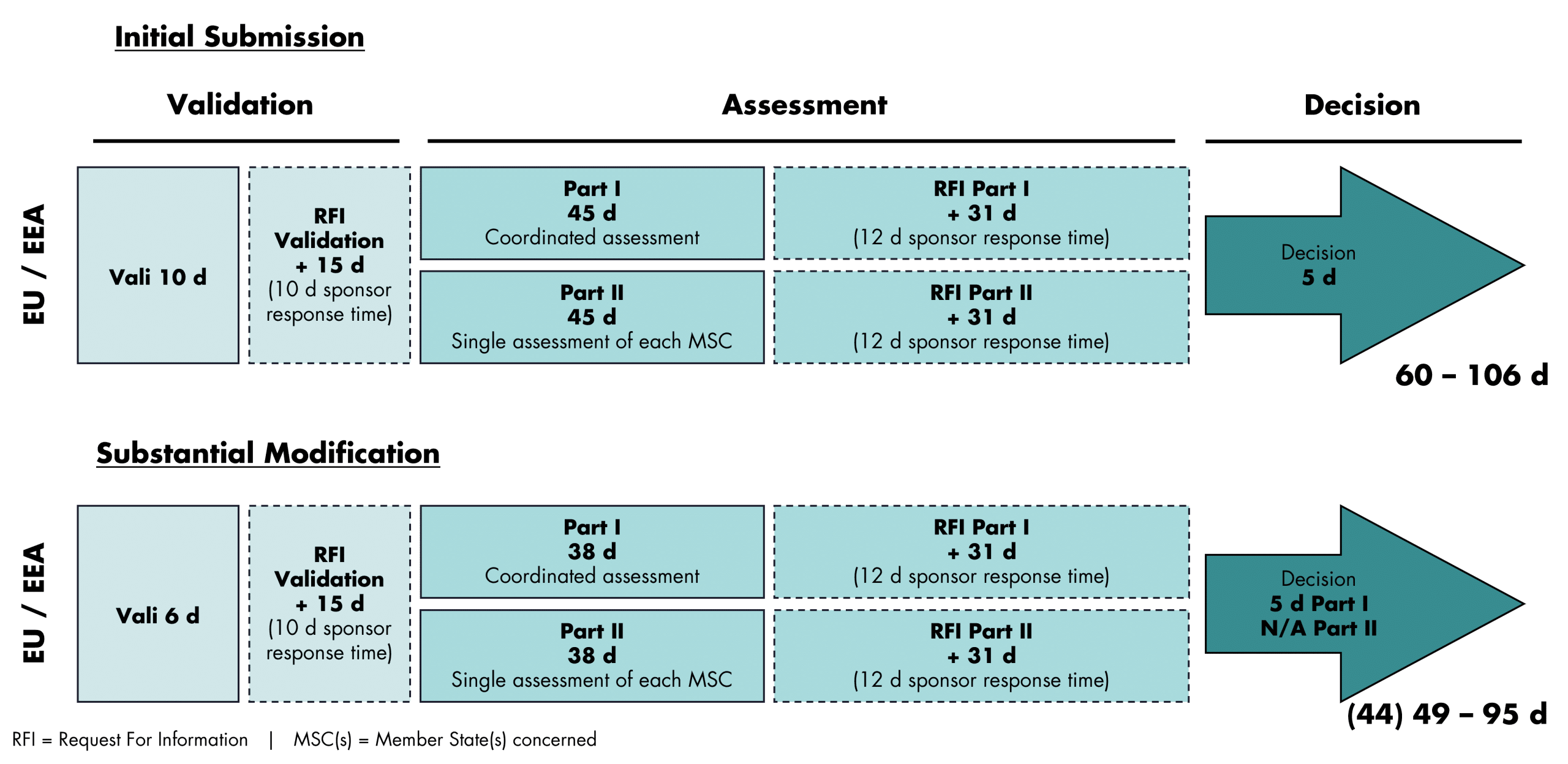
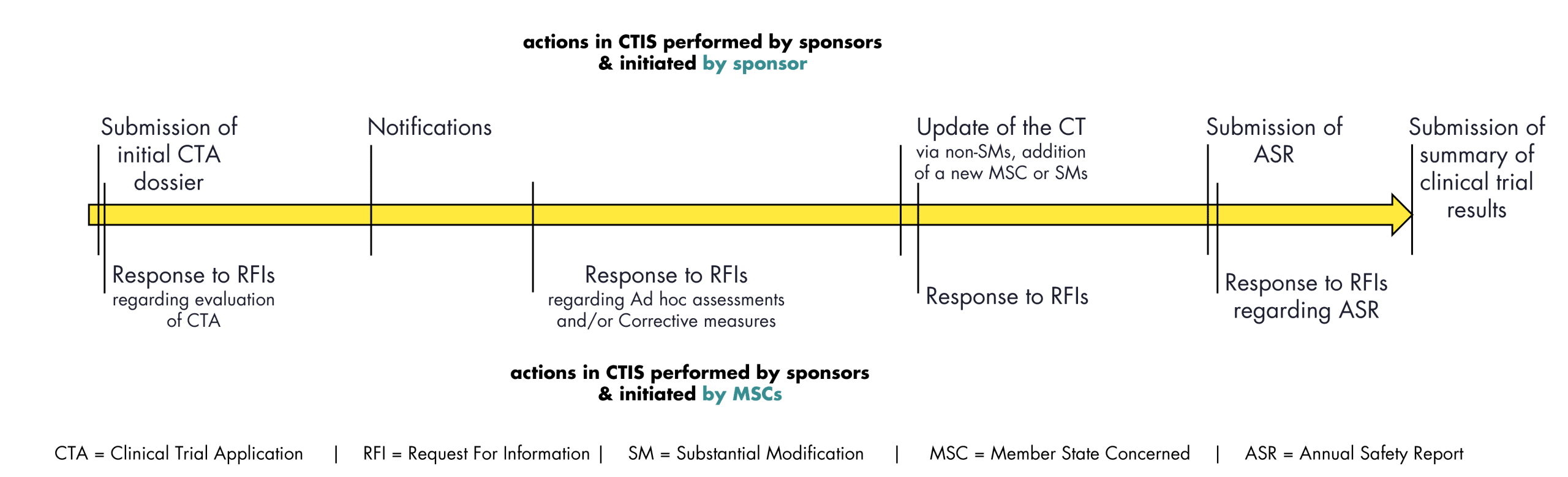
Regulatorische Zeitpläne in CTIS